|
|
95+ Granisetron EP em pó branco Impuridade A CAS 127472-42-8
|
Detalhes do produto:
Condições de Pagamento e Envio:
|
| Nome do produto: | Granisetron EP Impuridade A | Número CAS: | - Não, não. |
|---|---|---|---|
| M.W.: | 312,41 | MF: | C18H24N4O |
| Aparência: | Pó branco | Purificação: | 95+ |
| EINECS Não: | - | Armazenamento: | 5-25°C |
| Destacar: | 95 Granisetron EP Impuridade A,Granisetron EP Impuridade A 127472-42-8,95 Granisetron EP Impuridade A |
||
Descrição do produto
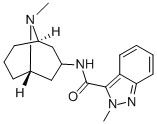
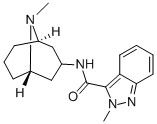
Granisetron EP em pó branco Impuridade A CAS 127472-42-8 95+
Nome:Granisetron EP Impuridade A
CAS NO:- Não, não.
M.W.:312.41
Aparência: Pó branco
Purificação: 95+
Sinônimos:Granisetron EP Impuridade A
Aplicação
Controle e garantia da qualidade: O controlo da presença e quantidade de Granisetron EP Impuridade A é crucial para garantir a pureza e qualidade do Granisetron.Serve de indicador-chave no processo de controlo da qualidade, permitindo aos fabricantes avaliar se o medicamento cumpre as normas regulamentares e garante a sua segurança para os doentes.As equipas de controlo de qualidade podem manter a consistência e a fiabilidade do produto final.
Pesquisa e Desenvolvimento de Medicamentos: Estudar a Impuridade do Granisetron EP A pode fornecer insights valiosos para pesquisadores e desenvolvedores que trabalham na melhoria da síntese e formulação do Granisetron.Compreensão dos mecanismos de formação, reatividade e propriedades farmacológicas potenciais desta impureza podem ajudar a otimizar o processo de produção, melhorar a estabilidade do medicamento e potencialmente descobrir novos benefícios terapêuticos..
Monitorização do processo de produção: o monitoramento da impureza do Granisetron EP A durante a produção do Granisetron ajuda os fabricantes a identificar potenciais problemas no processo de produção,tais como a contaminação das matérias-primas ou reacções incompletasAo detectar esta impureza, os engenheiros podem ajustar prontamente os parâmetros de produção ou introduzir medidas corretivas para garantir a qualidade do produto e manter uma elevada eficiência de produção.
Pacote
![]()
![]()
![]()
![]()
Transportes
Pequenos pacotes ((1g, 25g, 1Kg, 25Kg) podem ser enviados por Express. (DHL, FedEx, EMS, etc.)
Os grandes pacotes ((100kg e mais de100Kg) podem ser transportados por via aérea ou marítima.
Todo o transporte é de acordo com as necessidades do cliente.
Perfil da empresa
![]()
![]()
![]()
![]()
![]()
![]()
Pessoa de Contato: admin
-
98+ Impuridades em pó branco ((Normas) 6-Cloro-N-Metilpiridina-2-Carboxamida CAS 845306-04-9
-
98+ Pó branco TICAGRELOR CAS 1129683-88-0 C14H14N4O3
-
98+ Impuridades do pó branco ((Normas) Impuridade do sorafenib 16 CAS 2206827-12-3
-
98+ Pó branco Sorafenib Composto relacionado 8 NO. 1431697-81-2 CAS
-
98+ Pó branco Sorafenib Impuridade 6 CAS 1285533-84-7
-
Puro 98+ Branco em pó Sorafenib Impuridade 3 CAS NO. 284670-98-0 C27H24N6O5